Odkrycie w immunologii, a leczenie nowotworów
Tytuł doniesienia w BBC brzmi: Immune discovery ‘may treat all cancer’ [Odkrycie w immunologii „może leczyć wszystkie rodzaje nowotworów”]. Większość tytułów w mediach (także o prawdziwych odkryciach naukowych), ma tendencję do wielkiej przesady. Wszystkie odkrycia w medycynie najwyraźniej albo wyleczą każdego raka, albo przeziębienie. Moim zdaniem, ten tytuł także jest przesadzony, ale jest to prawdziwe odkrycie z możliwymi implikacjami dla przyszłych terapii nowotworów.
Naukowcy odkryli receptor układu odpornościowego, który wydaje się celować w większość komórek nowotworowych, nie atakując równocześnie zdrowych komórek. To z pewnością wydaje się być obiecujące do wykorzystania w immunoterapii nowotworów. Tytuł samego badania brzmi: Genome-wide CRISPR–Cas9 screening reveals ubiquitous T cell cancer targeting via the monomorphic MHC class I-related protein MR1.
Interesujący jest tu CRISPR, czego nie wspomina artykuł BBC. Jest to kolejny przykład, jak CRISPR turbodoładowuje badania genetyczne. Badacze użyli tej metody do przeczesania genomu i znaleźli receptor na limfocytach T, MR1, który wydaje się atakować nowotworowe komórki, ale nie atakuje zdrowych komórek. Ponadto ten atak wydaje się odbywać poprzez metabolizm komórki nowotworowej. W jakiś sposób ten receptor wyczuwa zmieniony metabolizm komórki nowotworowej. Co ważne, celuje w cechę metabolizmu, która jest powszechna dla większości, jeśli nie dla wszystkich, rodzajów nowotworów:
“Zespół z Cardiff odkrył limfocyt T i jego receptor, który w laboratorium potrafi znaleźć i zabić szeroki wachlarz nowotworowych komórek, włącznie z komórkami raka płuc, skóry, krwi, okrężnicy, piersi, prostaty, jajników, nerek i szyjki macicy”.
W tym miejscu muszę podkreślić, że to jest podstawowe badanie naukowe, nie zaś badanie kliniczne. To jest także sam początek badania, co znaczy, że otwiera to długą listę dalszych badań nad pytaniami, na które trzeba znaleźć odpowiedzi. Pracuję w tej dziedzinie wystarczająco długo, by mieć pojęcie o tym, gdzie badanie jest na łuku postępu od czystej nauki do zastosowań klinicznych. O immunoterapiach nowotworów, które zaczęły pojawiać się w ostatnich kilku latach, słyszałem po raz pierwszy w latach 1990.Typowe jest 20-30-letnie opóźnienie od momentu, kiedy badanie podstawowe sugeruje możliwą terapię, do zaaprobowania tej terapii do klinicznego użycia. Tempo może obecnie być nieco szybsze z powodu technologii badań podstawowych. Kliniczne badania jednak po prostu muszą zabierać czas. CRISPR jest tego znakomitym przykładem. Potrzebne jest przejście od badań na zwierzętach do wieloetapowych badań na ludziach nawet dla jednego wskazania użycia. Konieczne są kolejne badania, by lepiej zrozumieć jak terapia działa, na które choroby i na jakich pacjentów.
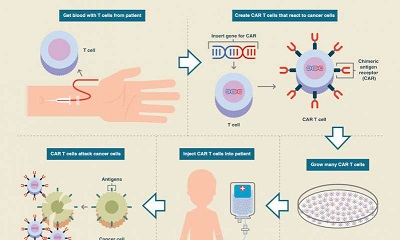
Dobrą wiadomością dla tego nowego odkrycia jest to, że podstawowa technologia już jest używana – immunoterapia nowotworów. W zasadzie jesteśmy więc już w połowie drogi. Może więc 10-15 lat jest bardziej optymistyczną oceną, jeśli wszystko pójdzie dobrze. Istnieje już kilka rodzajów immunoterapii nowotworów, które dotyczą wzmocnienia lub nacelowywania układu odpornościowego, by lepiej zwalczał nowotwór. Dla tego nowego odkrycia najbardziej istotna jest terapia limfocytami T o nazwie CAR (chimeryczne receptory antygenowe). Ten rodzaj immunoterapii polega na pobieraniu krwi pacjenta z nowotworem, a następnie odfiltrowywaniu limfocytów T. Następnie używa się wirusa do wstawienia genu do limfocytu T, dostarczającego receptora, który atakuje specyficzny rodzaj nowotworu danego pacjenta. Na przykład, używa się receptora CD19 przy białaczce i chłoniakach. Inne receptory będą potrzebne, by celować w inne rodzaje nowotworów.
Tutaj przełomem wydaje się więc fakt, że badacze znaleźli receptor, który wydaje się pasować do wszystkich rodzajów nowotworów – a przynajmniej tych, które przetestowali. Teoretycznie więc możemy użyć podejście CAR, ale używać receptora MR1 zamiast receptorów specyficznych dla danego rodzaju nowotworu. Oczywiście, można zrobić jedno i drugie w nadziei na zsumowanie się efektów. Ale terapia CAR T MR1 teoretycznie mogłaby być stosowana do każdego rodzaju nowotworu.
Nadal jest tu jednak jeden wielki szkopuł – terapia CAR T jest bardzo skuteczna przy leczeniu nowotworów krwi, ale niezbyt skuteczna przy solidnych guzach. Prawdopodobnie jest to praktyczny efekt zdobywania przez CAR T-komórki dostępu do komórek nowotworowych, ale mogą tam być jeszcze inne przeszkody. To jest obecnie dziedzina energicznych badań. Jest to więc wyraźny problem, który trzeba rozwiązać, zanim terapia CAR T z MR1 będzie mogła stać się naprawdę uniwersalną terapią nowotworów.
I jeśli historia jest tu przewodnikiem, to tym, co się na ogół zdarza, jest to, że nowa terapia nowotworów brzmi przy wprowadzaniu jak możliwość wyleczenia nowotworów, a potem staje się ważnym, dodatkowym leczeniem w arsenale onkologii, ale jest tylko jednym, kolejnym, niewielkim krokiem naprzód. Nie wątpię, że to nowe odkrycie doda coś wartościowego do naszej technologii leczenia nowotworów. Pytanie brzmi: jak będzie skuteczne i jak naprawdę uniwersalne będzie jego zastosowanie?
Oczywiście mam nadzieję, że będzie przełomem, który naprawdę wyleczy wszystkie rodzaje nowotworów, ale historia podpowiada ostrożność. Realistycznie rzecz biorąc, mam nadzieję, że okaże się to dość dużym krokiem naprzód.
NeuroLogica blog, 21 stycznia 2020
Tłumaczenie: Małgorzata Koraszewska
Neurolog, wykładowca na Yale University School of Medicine. Przewodniczący i współzałożyciel New England Skeptical Society. Twórca popularnych (cotygodniowych) podkastów o nauce The Skeptics’ Guide to the Universe. Jest również dyrektorem Science-Based Medicine będącej częścią James Randi Educational Foundation (JREF), członek Committee for Skeptical Inquiry (CSI) oraz członek założyciel Institute for Science in Medicine. Prowadzi blog Neurologica.