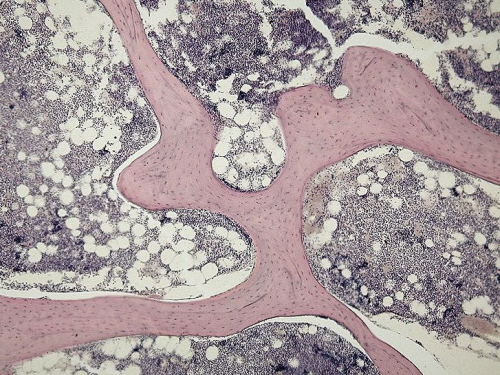
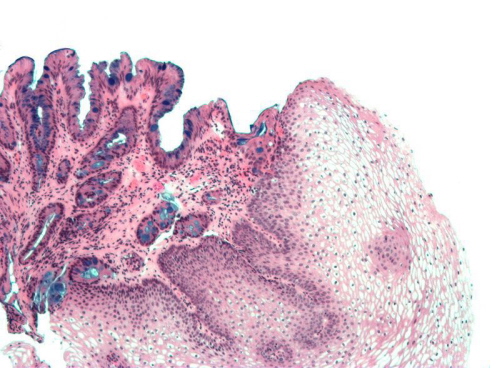
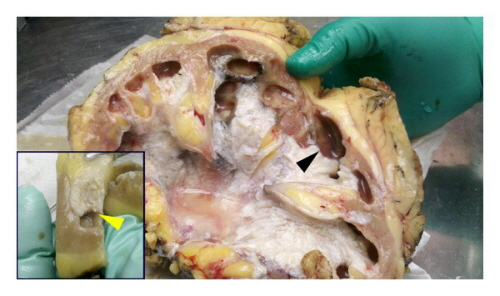
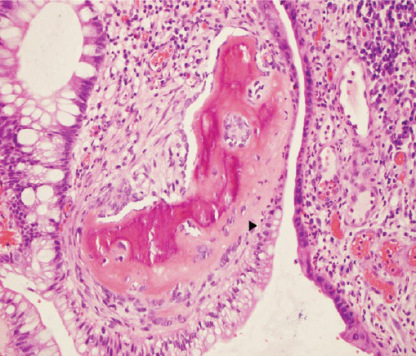
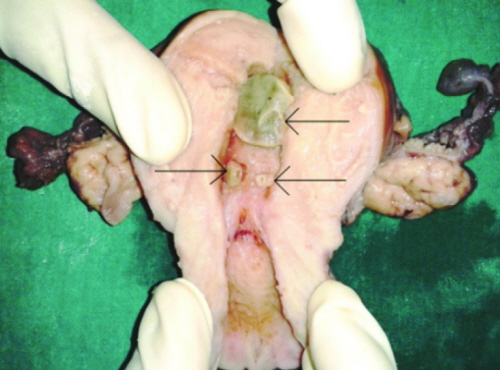
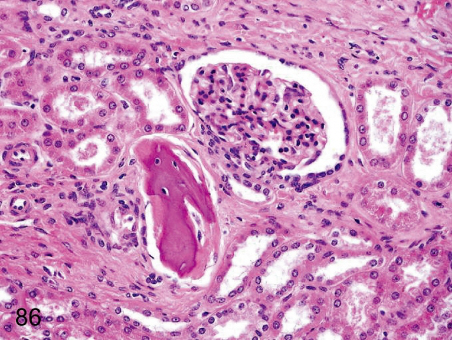
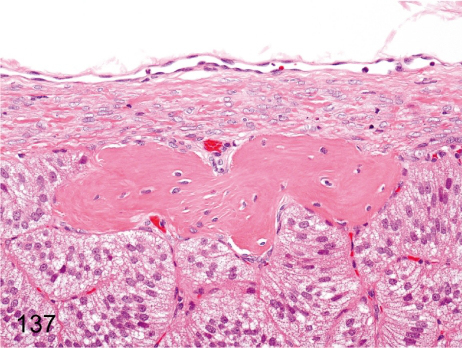
Kości! Wszędzie kości!
Metaplazja zatem. Najprościej mówiąc – przemiana jednej dojrzałej tkanki w inną. Na przykład nabłonka płaskiego w gruczołowy albo odwrotnie, gruczołowego w płaski tudzież zwykłego nabłonka gruczołowego żołądka w nabłonek jelitowy lub tkanki włóknistej w tkankę chrzęstną bądź kostną właśnie. Brzmi dziwnie? Tak naprawdę rzecz jest trochę mniej zaskakująca niż mogłoby się w pierwszej chwili wydawać. Metaplazja nie polega bowiem zwykle wcale na bezpośredniej zmianie samych dojrzałych komórek (o czymś takim mówimy podczas procesu zwanego transdyferencjacją) – to raczej zaburzenie ich różnicowania. Poza dojrzałymi komórkami odpowiedzialnymi za ich strukturę i funkcję poszczególne tkanki zaopatrzone są też w pewną pulę komórek niedojrzałych/niezróżnicowanych odpowiedzialnych chociażby za odbudowę po poważniejszych uszkodzeniach. Taką pulę rezerwową. I to ta pula rezerwowa właśnie w pewnych warunkach zamiast odtwarzać oczekiwany w danej lokalizacji typ tkanki zaczyna dojrzewać w zupełnie innym kierunku.
W licznych przypadkach najczęściej spotykanej metaplazji nabłonkowej jesteśmy w stanie zidentyfikować przyczyny, które do przemiany doprowadziły. Zazwyczaj kluczowym bodźcem jest przewlekłe drażnienie – urazy mechaniczne, infekcje, etc. Nowe, inaczej zróżnicowane komórki mają być odporniejsze na uciążliwe warunki (metaplazję zwykle opisuje się jako zmianę adaptacyjną).
Tak jest chociażby gdy podczas przewlekłej choroby refluksowej przełyku cofająca się kwaśna treść żołądkowa nieustannie podrażnia zwykły wielowarstwowy nabłonek płaski przełyku, z czasem u niektórych chorych doprowadzając do zastąpienia go nietypowym dla tego narządu nabłonkiem gruczołowym (jednowarstwowym walcowatym z metaplazją jelitową) i powstania patologii nazywanej przełykiem Barretta (tak, znów eponimy). Podobnie wygląda reakcja śluzówki żołądka na przewlekłe zapalenie – z czasem nabłonek gruczołowy żołądka przekształca się w nabłonek jelitowy. W pęcherzu moczowym z kolei nawracające infekcje przyczyniają się do przemiany nabłonka przejściowego (typowego dla całych dróg moczowych) w nabłonek wielowarstwowy płaski rogowaciejący przypominający strukturą naskórek. Przykłady można zresztą długo mnożyć – zmiany metaplastyczne w obrębie poszczególnych typów nabłonków obserwujemy także w nabłonku oddechowym oskrzeli, błonie śluzowej szyjki i trzonu macicy, pęcherzyku żółciowym, etc. Tego typu przemiany są dość intensywnie badane, jako że część spośród nich wiąże się ze znacznym podwyższeniem ryzyka nowotworzenia – tu najistotniejsze są prawdopodobnie procesy zachodzące w żołądku, przełyku i oskrzelach. Znamy już przynajmniej niektóre kierujące zmianami ścieżki molekularne, wiemy coraz lepiej jak w danych sytuacjach klinicznych postępować.
Nieco inaczej sytuacja wygląda dla metaplazji innych niż nabłonkowe (przykładowo kostnej właśnie). Tu wiemy znacznie mniej. Przede wszystkim niejasne są już same przyczyny zmian. Niekoniecznie uznaje się je za adaptację do czegokolwiek, niekiedy wprost określa się je mianem zmian degeneracyjnych po prostu, choć niektóre przypadki udaje się niekiedy powiązać z różnego typu urazami tudzież procesami zapalnymi. Nie uważa się też, by można je było uznać z wstęp do rozwoju nowotworów, choć wtórnie w przebiegu niektórych chorób nowotworowych można obserwować ogniska przemiany kostnej. Wydają się dużo mniej powszechne niż przemiany różnych typów tkanek nabłonkowych, równocześnie jednak bywają dużo bardziej spektakularne. Inne w końcu wrażenie wywiera inny niż spodziewany w danej lokalizacji nabłonek, inne – kawał kości w miejscu, w którym żadnych kości być nie powinno.
Ot, wspomniany na początku polip trzonu macicy. Macica zasadniczo nie powinna zawierać kości. OK, od czasu do czasu mogą się pojawić pewne niespodzianki, w przypadku pewnych typów guzów, po terminacji ciąży lub niepełnych poronieniach chociażby, jednak nie mieści się to w standardzie. Tymczasem niekiedy można się zdziwić. Czy to w polipie, czy w mięśniaku, czy po prostu ogniskowo w obrębie niezmienionej poza tym błony śluzowej obszary kostnienia można rzadko (mówi się o mniej więcej 3 przypadkach na 10 000 badań) odnaleźć – w wyjątkowych przypadkach nie tylko samego zresztą kostnienia, ale nawet towarzyszącego mu utkania szpiku kostnego z krwiotworzeniem. Niestety, mimo iż rzecz nie predysponuje do rozwoju nowotworu, niekoniecznie jest znaleziskiem obojętnym – zupełnie jak wkładka wewnątrzmaciczna może upośledzać zagnieżdżenie się zarodka, może też utrudniać późniejsze utrzymanie ciąży. Bywa też przyczyną zaburzeń miesiączkowania, gdy pojawi się w obrębie śluzówki szyjki macicy może przyczyniać się do krwawień i bolesności towarzyszącej stosunkom seksualnym. A skąd się bierze? Nie wiadomo. Owszem, w części przypadków można się doszukać wcześniejszych urazów, zwłaszcza aborcji, ale przecież nie we wszystkich, a w tych, w których się doszukano, odstęp czasowy sięgający nawet kilkunastu lat czyni związek przyczynowo-skutkowy nieszczególnie prawdopodobnym. Czasem ogniskom towarzyszy naciek zapalny czy zmiany degeneracyjne, ale wcale nie zawsze. Prawdopodobnie zjawisko jest zbyt rzadkie, byśmy dali radę dojść do jednoznacznych wniosków.
Podobnie w innych częściach ciała. Choć poszczególne przypadki są dobrze znane, niewiele można powiedzieć o ich etiologii, przynajmniej po części ze względu na rzadkość zjawiska. Prowadzono kilka badań nad mechanizmami metaplazji kostnej w obrębie nowotworów jelita grubego, doszukując się udziału w procesie pewnych z tkanką kostną powiązanych czynników wzrostu hipotetycznie wytwarzanych przez komórki sąsiadujące z badanymi zmianami, jednak dane nadal są niestety raczej skąpe i nierozstrzygające. Tymczasem literatura medyczna notuje obecność przemiany kostnej nie tylko w obrębie zapalnych czy nowotworowych zmian jelita, ale też w polipach zapalnych nosa, łagodnych zmianach rozrostowych tarczycy czy zmienionych miażdżycowo naczyniach tętniczych (tu akurat mechanizmy są nieco lepiej poznane z całym szeregiem zaangażowanych czynników transkrypcyjnych i czynników wzrostu – choroby układu krążenia nie bez powodów budzą żywe zainteresowanie współczesnej medycyny). Zresztą nie tylko “ludzka” literatura medyczna.
Metaplazję kostną czy to w nerkach, czy w nadnerczach, czy też na przykład oskrzelach bądź śliniankach obserwowano także u zwierząt zarówno tych laboratoryjnych, jaki i zwykłych pacjentów klinik weterynaryjnych, nic w tym w sumie dziwnego patologia weterynaryjna, choć na niektórych polach odmienna, ma z “człowieczą” wiele wspólnego. Zwłaszcza gdy idzie o niespodzianki, które obie mogą przynieść medykom zmagającym się z codzienną diagnostyką. W końcu kto spodziewałby się kości w tęczówce?
(Przypominam tylko, że patologów możecie śledzić też na fejsbuku)
Literatura:
Metaplasia and transdifferentiation: from pure biology to the clinic. JMW Slack; Nature Reviews Molecular Cell Biology 2007; 8:369-378
Postępowanie w przełyku Barretta. Aktualne stanowisko American Gastroenterological Association. Ł Strzeszyński dla Medycyny Praktycznej na podstawie: American Gastroenterological Association, Spechler S.J., Sharma P., Souza R.F., Inadomi J.M., Shaheen N.J. i wsp.: American Gastroenterological Association medical position statement on the management of Barrett’s esophagus, Gastroenterology, 2011; 140: 1084–1091
Epithelial metaplasia and the development of cancer. JM Quinlan, BJ Colleypriest, M Farrant, D Tosh; Biochimica et Biophysica Acta (BBA) – Reviews on Cancer 2007; 1776(1):10–21
Epidemiology of Premalignant Gastric Lesions: Implications for the Development of Screening and Surveillance Strategies. AC De Vries, EJ Kuipers; Helicobacter 2007;
Metaplastic conditions of the bladder. D Clouston, N Lawrentschuk; BJU International 2013; 112(S2):27–31
Keratinizing Squamous Metaplasia of the Bladder: A Review. I Ahmad, RJ Barnetson, NS Krishna; Urologia Internationalis 2008; 81 (3):247–251
Endometrial Osseous Metaplasia: Case Report with Literature Review. SB Patil, S Narchal, DG Paricharak, SS More; Annals of Medical and Health Sciences Research 2013; 3(Suppl1):S10–S12
Endometrial osseous metaplasia: Clinicopathological study of a case and literature review. T Umashankar, S Patted, RS Handigund; Journal of Human Reproductive Sciences 2010; 3(2):102–104
Osseous Metaplasia in an Inflammatory Polyp of the Rectum: A Case Report and Review of the Literature. B Odum, ML Bechtold, A Diaz-Arias; Gastroenterology Research 2012; 5(2):74-8
Regulatory Mechanisms in Atherosclerotic Calcification. AP Sage, Y Tintut, LL Demer; Nature Reviews Cardiology 2010; 7:528-536
Lekarka ze specjalizacją z patomorfologii, pasjonatka popularyzacji nauki, współtwórczyni strony poświęconej nowinkom naukowym Nauka głupcze, ateistka, feministka. Prowadzi blog naukowy Patolodzy na klatce. (Wszystkie publikowane tu teksty Pauliny Łopatniuk ukazują się najpierw na jej blogu.)