Norowirus: doskonały patogen wyłania się z cienia
Niezdolność hodowania norowirusów spowodowana jest z kolei naszą ignorancją o niektórych najważniejszych aspektach ich biologii. Naukowcy wiedzą, że wirus atakuje przewód pokarmowy, ale nie wiedzą na pewno, jaki rodzaj komórek atakuje ani jak właściwie to robi. Wiedzą, że chociaż norowirus nie powoduje żadnej choroby krwi, różne norowirusy są bardziej niebezpieczne dla ludzi z różnymi grupami krwi.
Obecnie jednak grupa naukowców kierowana przez Stephanie Karst z University of Florida prawdopodobnie przebiła się przez wiele z tych tajemnic. Karst z kolegami odkryli jak norowirusy dostają się do naszych komórek. Okazało się, że pomagają im niektóre z naszych nieszkodliwych bakterii jelitowych.
Przez lata naukowcy zakładali, że norowirusy infekują komórki, które stanowią wewnętrzną wyściółkę jelit. Przecież te właśnie komórki (komórki nabłonkowe) są pierwszymi, jakie spotykają wirusy, kiedy dostają się do przewodu pokarmowego.
Gdyby norowirusy zakażały komórki nabłonkowe, naukowcy mogliby również wyjaśnić zaskakujący związek z grupami krwi. Nasze grupy krwi są określone przez rodzaj węglowodanów, które ozdabiają nasze czerwone krwinki. Ale także nasze komórki nabłonkowe w jelitach nakładają na swoje powierzchnie te same węglowodany. Norowirusy mogą wiązać się z tymi węglowodanami (znanymi oficjalnie jako antygeny grup krwi czyli HBGA).
Dodaj wszystkie dowody i masz dość prosty scenariusz: norowirusy dostają się do jelit, przyczepiają do HBGA na komórkach nabłonkowych, najeżdżają te komórki i – proszę bardzo – mamy kilka dni wymiotowania i biegunki.
Choć ten scenariusz brzmiał bardzo sensownie, był z nim jeden duży problem: kiedy naukowcy przeprowadzali eksperymenty, wirusy nie wykazywały żadnego zainteresowania komórkami nabłonkowymi. Ani nie wydawały się pozostawać na powierzchni jelit. Zespół Karst zainfekował myszy mysią wersją norowirusa i odkrył, że wirus jakoś wkopał się głęboko w wyściółkę jelitową.
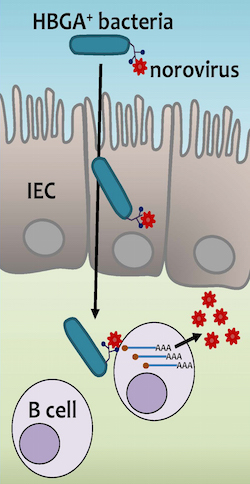
Zagrzebane głęboko w wyściółce naszych jelit są kieszonki komórek odpornościowych, które chronią nas przez infekcjami jelitowymi. Kiedy pokarm przechodzi przez jelita, komórki nabłonkowe wychwytują podejrzanie wyglądające białka i dostarczają do tych kieszonek. Komórki, znane jako komórki B, mogą wtedy wytworzyć przeciwciała, które atakują niebezpieczne patogeny.
To głębokie nurkowanie uprawiane przez norowirusy nasunęło podejrzenia, że zakażają one komórki B w jelitach. Zainteresowanie zespołu Karst komórkami B wzrosło jeszcze bardziej po przeprowadzeniu kolejnego eksperymentu na myszach. Naukowcy mieli nadzieję, że uda się zrozumieć, jak zakażenie norowirusami może chronić mysz przed dalszymi infekcjami. Jako część eksperymentu wyhodowali myszy, które nie potrafiły wytwarzać komórek B.
Można by oczekiwać, że myszy będą mniej odporne na zakażenie norowirusem, ponieważ nie mogą wytwarzać przeciwciał. Prawdą jest jednak odwrotność: bez komórek B myszy stały się odporniejsze.
Zastanawiając się nad tym wszystkim Karst i jej koledzy zaczęli podejrzewać, że, być może, prawdziwym celem norowirusów nie były komórki nabłonkowe, ale komórki B.
Sprawdzili ten pomysł na mysich norowirusach. Kiedy mieszali mysie norowirusy z mysimi komórkami B w probówce, wirusy istotnie potrafiły wniknąć do komórek, jak to podejrzewali naukowcy. Kiedy jednak próbowali zainfekować komórki nabłonkowe, wirusom nie udawało się w nie wniknąć.
Oczywiście badacze nie mogli być pewni, że to, co jest prawdą dla myszy, dotyczy także ludzi. Jednak testowanie ich koncepcji na ludzkich norowirusach byłaby dużo trudniejsze, bo Karst nie miała nieskończonego zapasu czystych norowirusów.
Zamiast tego badacze musieli zbierać próbki kału od chorych pacjentów. Rozcieńczali pełen wirusów kał i mieszali go z ludzkimi komórkami B. Tak jak się spodziewali wirusy zakażały komórki B.
Był tam jednak fascynujący haczyk. Jeśli naukowcy przepuszczali kał przez bardzo drobne filtry – wystarczająco drobne, by nie przepuścić bakterii – norowirusy nie potrafiły dłużej infekować komórek B.
Sugerowało to, że bakterie jelitowe – a przynajmniej jeden gatunek bakterii – pomagały norowirusom.
Byłoby absurdem, gdyby zespół Karst zabrał się za testowanie każdego gatunku bakterii jelitowych, żeby zobaczyć, która pomaga norowirusom. Nasze wnętrzności zawierają setki gatunków. Na szczęście, wcześniejsze badania innych naukowców pozwoliły Karst i jej zespołowi uniknąć taktyki sprawdzania wszystkiego.
Okazuje się, że komórki krwi i komórki nabłonkowe nie są jedynymi, które produkują cząsteczki grup krwi. Pewne gatunki bakterii także mają HBGA. Nie jest jasne, dlaczego mają te same cząsteczki, co my. Jakikolwiek jednak jest powód, norowirusy mogą złapać się bakteryjnych HBGA.
Zespół Karst wybrał jeden z gatunków, które potrafią wiązać norowirusy. Jest to pospolity rodzaj bakterii o nazwie Enterobacter cloacae. Badacze dodali Enterobacter cloacae do przefiltrowanych próbek kału, które zawierały ludzkie norowirusy. A potem połączyli tę mieszankę z ludzkimi komórkami B. Teraz udało się zainfekować komórki B ludzkimi norowirusami.
Ten eksperyment nie ujawnia jak Enterobacter cloacae pomaga norowirusom dostać się do komórek B. Jest możliwe, że bakterie przenoszą je do ukrytych kieszonek, gdzie czają się komórki B. Jest także możliwe, że kiedy wirusy przyczepiają się do bakterii, powiązanie wywołuje zmianę na powierzchni cząsteczek, umożliwiając im zainfekowanie komórek. Karst ma nadzieję na znalezienie odpowiedzi na te pytania w dalszych badaniach.
Te nowe wyniki mogą jednak dostarczyć wyjaśnienia, dlaczego grupa krwi ludzi powoduje, że jedni są bardziej a inni mniej podatni na norowirusy. Powiedzmy, że masz grupę krwi B. Twój układ odpornościowy uczy się rozpoznawać typ B HBGA jako nieszkodliwy, ponieważ są one częścią twojego ciała. Jest możliwe, że jeśli zostajesz skolonizowany przez bakterie, które także mają B HBGA, twój organizm będzie je tolerował.
Jeśli jednak zarazisz się bakterią, która nosi typ A HBGA, twój układ odpornościowy może wytworzyć przeciwciała i zaatakować je jako obcych. To jest prawdopodobnie przyczyna, dla której transfuzja krwi niewłaściwej grupy może być tak niebezpieczna. Jeśli masz grupę B, masz wiele przeciwciał typu A HBGA. Więc twój organizm zaatakuje krew grupy A jako obcą.
Nowe badanie zespołu Karst może także wyjaśnić, dlaczego norowirusy wydają się zważać na twoją grupę krwi. Twoja grupa krwi może określać rodzaj bakterii, która może żyć w jelitach – a więc rodzaj bakterii, do której mogą przyczepić się norowirusy i użyć ich, by dostać się do komórek B.
Byłoby wspaniale, gdyby można było powiedzieć, że to odkrycie bezpośrednio wskazuje na niezawodną kurację przeciwko niedoli spowodowanej przez norowirusy. Tak jednak niestety nie jest. Zespół Karst był w stanie zablokować infekcję norowirusową u myszy przez użycie antybiotyków, by wymieść ich bakterie jelitowe. Bez pomocy bakterii wirus nie mógł dostać się do komórek B. Ale ten rodzaj kuracji jest gorszy niż choroba. Mikrobiom wykonuje wiele ważnych zadań, włącznie z pomocą przy trawieniu i tworzeniem swego rodzaju bariery ekologicznej, która nie dopuszcza do inwazji paskudnych patogenów. Zniszcz go, a możesz bardzo się rozchorować – znacznie bardziej niż z powodu infekcji norowirusem.
Niemniej, to odkrycie nadal jest ważne, ponieważ wyjaśnia, dlaczego nie powodziły się poprzednie próby hodowania norowirusów. Wirusy otrzymywały zły cel i nie otrzymywały pomocy, jakiej potrzebowały, by weń uderzyć. Teraz Karst ma nadzieję, że jej zespół wreszcie stworzył przepis na wyhodowanie wielkich ilości ludzkich norowirusów do badań nad szczepionkami i lekami antywirusowymi.
I to jest jedyne znaczenie powiedzenia “mnóstwo norowirusów”, które może nas ucieszyć.
Norovirus the perfect pathogen emerges from the shadows
The Loom, 6 listopada 2014
Tłumaczenie: Małgorzata Koraszewska
Wielokrotnie nagradzany amerykański dziennikarz naukowy publikujący często na łamach „New York Times” „National Geographic” i innych pism. Autor 13 książek, w tym „Parasite Rex” oraz „The Tanglend Bank: An introduction to Evolution”. Prowadzi blog The Loom publikowany przy „National Geographic”.